 정지호 기자
정지호 기자
질병관리본부는 국내생산 탄저백신 개발을 위해 질병관리본부 용역사업으로 수행된 임상2상 시험의 안전성 및 유효성 결과가 지난 5월 28일 백신분야 저명 저널인 백신에 게재됐다고 밝혔다.
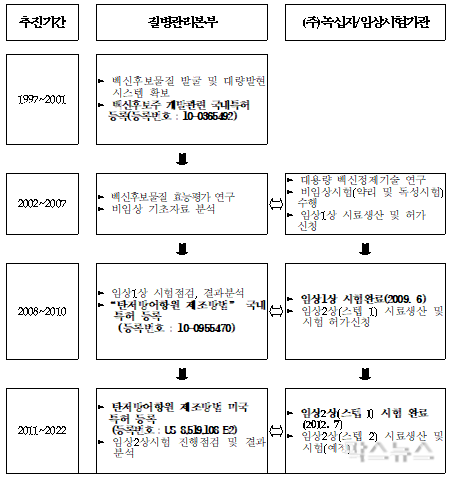 탄저백신 개발 추진현황. (사진 = 질병관리본부 제공)
탄저백신 개발 추진현황. (사진 = 질병관리본부 제공)
질병관리본부는 1998년 탄저백신후보 물질 및 생산균주를 자체개발해 특허를 취득한 바 있으며, 2002년부터 녹십자를 통해 용역사업으로 생산공정개발 및 비임상시험 등 제품화를 수행해 서울대학교병원에서 2009년 임상1상, 2012년 임상2상 시험을 완료했다.
임상2상 시험에서는 건강한 성인 104명을 대상으로 백신접종 후 주사부위 통증, 두통, 발열, 복통, 오한과 같은 안전성 평가와 백신접종군에서 형성된 항체 측정을 통한 효능평가가 실시됐다.
안전성 평가 결과, 백신접종군의 부작용 발생률은 위약군과 차이가 없으며 접종 후 탄저감염에 대한 방어항체가 형성됨이 확인됐다.
개발된 탄저백신은 탄저균의 방어항원을 주성분으로 한 재조합백신으로 대량생산 효과가 뛰어난 비병원성균주인 바실러스 브레비스를 발현시스템으로 사용함에 따라 안전성이 확보되고 경제성도 높을 것으로 예상되고 있다.
탄저는 사람 및 가축에서 발생되는 인수공통감염병으로 생물테러 등에 악용될 가능성이 높아 이에 대한 국가적 대비가 필요한 상황이다.
다른 곳에 퍼가실 때는 아래 고유 링크 주소를 출처로 사용해주세요.
 http://paxnews.co.kr/news/view.php?idx=4051
http://paxnews.co.kr/news/view.php?idx=4051